2022年终盘点 | NSCLC靶向治疗之EGFR篇
EGFR是肺癌常见的靶点,特别是针对EGFR 19del、21号外显子L858R及T790M等经典突变,罕见突变包括G719X(ex18)、S768I(ex20)、L861Q(ex 21),其他罕见突变如18del、E709X、19ins和复合突变等。今天小编就为大家盘点一下EGFR突变NSCLC的治疗。
part·1
EGFR常见突变——
三代EGFR-TKI纷纷挺进一线
2003 年吉非替尼的问世,开启了第一代 EGFR 靶向药治疗 NSCLC 的时代篇章!一代药物吉非替尼、厄洛替尼、埃克替尼,二代药物阿法替尼、达克替尼,三代药物奥希替尼、阿美替尼、伏美替尼也接踵而来!
1.奥希替尼
2019年8月,基于FLAURA研究数据,中国NMPA正式批准奥希替尼用于EGFR敏感突变(19号外显子缺失或L858R突变)的NSCLC一线治疗。
FLAURA研究是一项国际多中心、随机、对照Ⅲ期临床研究,旨在评估奥希替尼单药(80mg PO QD,n=279)或标准EGFR-TKIs治疗(SoC,包括吉非替尼 250mg PO QD或厄洛替尼 150mg PO QD,n=277)一线治疗EGFR敏感突变阳性晚期NSCLC患者的疗效和安全性。
主要终点PFS首先达到阳性:无进展生存期达到18.9个月,相较对照组10.2个月,延长了8.7个月,HR=0.46,降低了54%的进展或死亡风险!
关键次要研究终点OS实现历史性突破达到阳性终点,在FLAURA研究中,尽管有1/3的使用一代TKI的患者耐药后交叉到了奥希替尼组(即对照组中1/3数据是一代/二代耐药后序贯奥希替尼的数据),但是最终的总生存时间,奥希替尼一线使用组仍然达到38.6个月,相比一代TKI组31.8个月的中位OS,延长了6.8个月的生存时间,具有显著统计学意义及临床意义(HR=0.799,P=0.0462)!两组3年生存率为54% vs 44%。
这是EGFR-TKI药物在EGFR阳性人群的首次OS突破!也表明1/2代+3代的序贯模式,在生存获益上并不及一线直接用三代TKI奥希替尼。
2.阿美替尼
阿美替尼是我国首个自主研发的三代表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI),因其独特的结构,更能透过血脑屏障。其Ⅲ期AENEAS研究结果惊艳众人!
AENEAS研究是一项评价阿美替尼作为一线治疗方案疗效和安全性的多中心、随机、双盲Ⅲ期研究。试验共纳入429例携带EGFR19外显子缺失或L858R突变的晚期NSCLC患者,并将他们1:1随机接受阿美替尼或吉非替尼治疗,治疗直至疾病进展或毒性不可耐受。
研究主要终点为无进展生存期(PFS),次要终点包括总生存(OS),客观缓解率(ORR),反应持续时间(DoR)和安全性。
研究结果显示,使用阿美替尼作为一线治疗的患者,无进展生存期(PFS)及持续缓解时间(DoR)均显著延长——mPFS 19.3个月 vs 9.9个月(HR 0.46 , P<0.0001),mDoR 18.1个月 vs 8.3个月(HR 0.38 , P<0.0001)。
安全性方面,尽管阿美替尼组治疗持续时间更长(中位463天vs 254天),但是皮疹、腹泻、AST/ALT升高和治疗相关严重不良事件(4.2% vs 11.2%)发生率更低。
3. 伏美替尼
今年7月,中国国家药监局(NMPA)官网公示,艾力斯医药的甲磺酸伏美替尼片(商品名:艾弗沙)新适应症已获得正式批准,用于具有表皮生长因子受体(EGFR)外显子19缺失(19DEL)或外显子21(L858R)置换突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的一线治疗。
伏美替尼获批一线治疗NSCLC的新适应症上市申请,是基于一项名为FURLONG的随机、双盲、阳性对照的多中心3期注册临床研究结果,旨在对比伏美替尼与吉非替尼一线治疗EGFR敏感突变的局部晚期或转移性非小细胞肺癌患者的有效性和安全性。
研究结果表明,伏美替尼治疗组的IRC评估的中位PFS为20.8(17.8-23.5)个月, 相比吉非替尼组11.1(9.7-12.5)个月,取得了具有统计学意义的改善, 风险比[HR] 0.44 (95%CI 0.34-0.58,p<0.0001),降低疾病进展或死亡风险56%。
part·2
EGFR难治突变——
迎来两款重磅新药
0.1% - 4%的肺癌患者也会发生EGFR外显子20插入突变(EGFR 20Ins),该突变对EGFR-TKI靶向治疗不敏感,因此被称之为难治突变。
1.amivantamab
2021年5月,FDA加速批准强生公司研发生产的EGFR/c-Met双抗Rybrevant (amivantamab-vmjw,JNJ-6732) 上市,用于治疗铂类化疗后进展的EGFR外显子20插入突变的转移性非小细胞肺癌(NSCLC)患者。这是FDA批准的首个针对该类突变的药物。
Amivantamab(JNJ-61186372)是靶向EGFR和cMet的双特异抗体,属于EGFR和MET双靶的单抗静脉输注型药物,与既往的EGFR口服TKI决然不同。该双抗采用1+1的非对称形式(IgG1),抗体的一个Fab结合cMet靶点,另外一个Fab结合EGFR靶点。带有两个单点突变的抗体先分别在两个细胞株中进行生产,并进行纯化。纯化后的两个单克隆抗体在体外按照一定比例混合,经过还原和氧化处理形成异源二聚体双特异抗体,且具有ADCC效应。
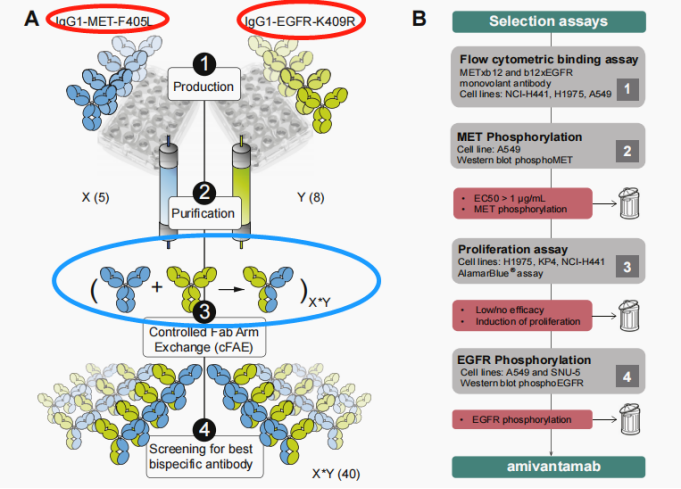
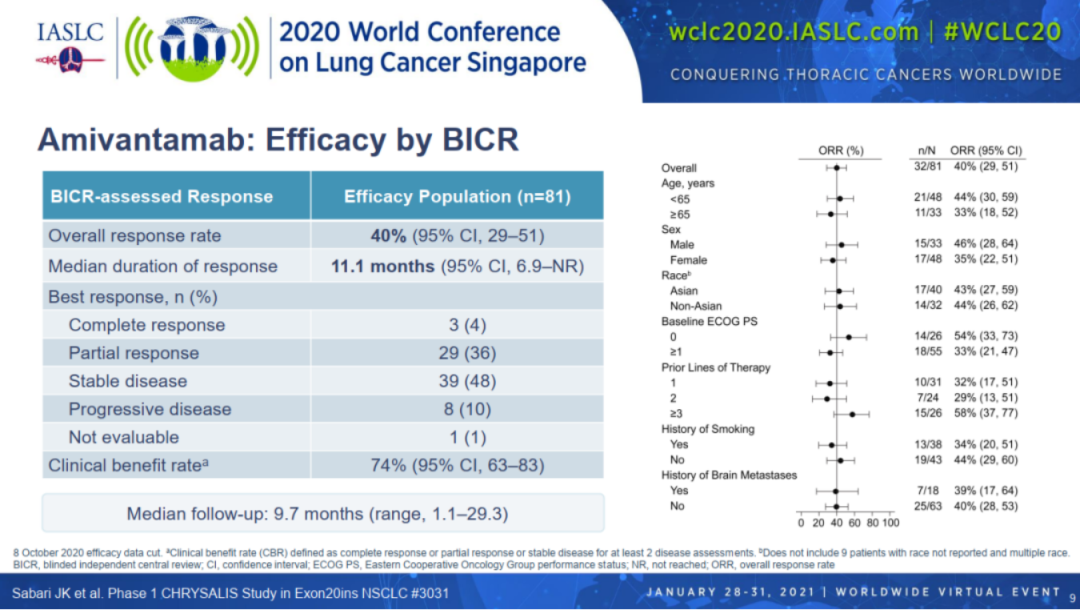
该批准是基于2020年WCLC会议上上更新的I期CHRYSALIS研究中amivantamab单药疗法队列的阳性结果,该研究共纳入81例既往接受过一线铂类化疗的EGFR 20ins的肺癌患者,疾病进展后均接受Amivantamab治疗。体重<80kg的患者接受1050 mg剂量,体重≥80 kg患者的剂量为1400 mg。
中位随访9.7个月后, 客观缓解率(ORR)为40%,其中完全缓解率CR为4%,部分缓解率PR为36%,中位缓解时间DoR为11.1个月。临床获益率(定义为在至少两次疾病评估中完全或部分缓解或疾病稳定)为74%。而20ins使用目前上市的1-3代TKI来说,疗效非常有限,10%以下。目前,Amivantamab联合化疗(培美曲塞+卡铂)一线治疗EGFR 20ins的NSCLC的III期研究PAPILLON(NCT04538664)正在进行,这是Amivantamab一线挑战EGFR 20ins标准化疗的大型开放标签、随机对照的III期研究。
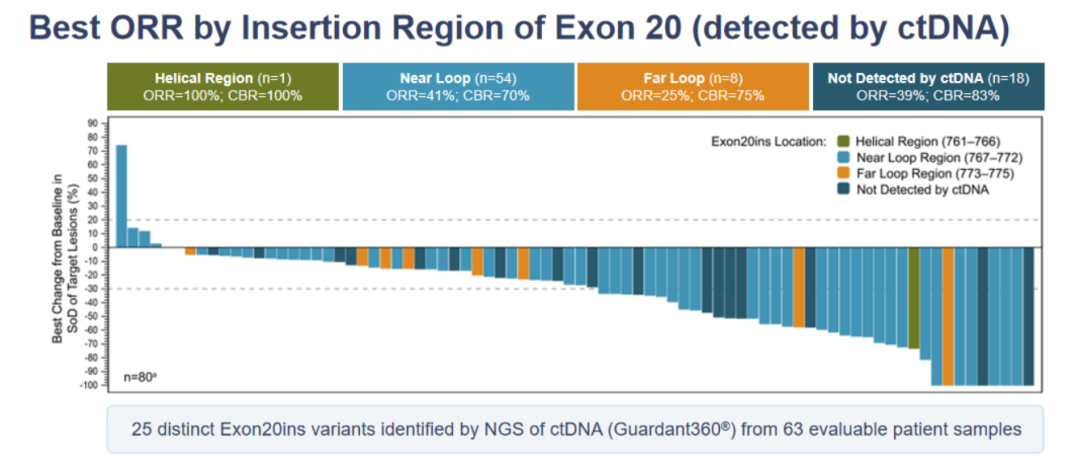
进一步分析显示,ctDNA或具有一定的疗效预测作用,Amivantamab对不同插入区域EGFR 20ins均被证实有效。其中Helical Region(n=1)ORR高达100%;Near Loop (n=54) ORR为41%;Far Loop(n=8) ORR为25%。
amivantamab在安全性方面基本可控,≥3级治疗相关不良反应发生率为16%,最常见的不良反应:皮疹,与输液有关的反应,指甲或脚趾甲周围的皮肤感染,肌肉和关节疼痛,呼吸急促,恶心,疲劳,小腿或手或面部肿胀,溃疡。口腔,咳嗽,便秘,呕吐和某些血液检查的变化。
2.mobocertinib
2021年9月15日,美国食品药物管理局(FDA)批准了武田制药的mobocertinib上市申请,适应症为用于治疗在含铂化疗治疗期间或治疗后进展的局部晚期或转移性的EGFR 20ins患者。Mobocertinib是武田研发的一种新型、高选择性、靶向 EGFR 20ins的口服酪氨酸激酶抑制剂(TKI),作为EGFR 20ins第二款获批药物,可以说是众望所归!
该决定是基于一项试验 NCT02716116 1/2 期的结果。
试验的第 1 部分采用剂量递增的 3+3 设计,纳入了 ECOG 体能状态低于2 的晚期 NSCLC 患者。其中6 名患者之前接受过铂类治疗。
在研究的第二部分,即扩展阶段,在以下 7 个队列中以 160 毫克的日剂量对莫博替尼进行了评估:
队列 1(n = 22):既往接受过铂类治疗、患有难治性EGFR外显子 20 插入阳性疾病且没有活动性、可测量的中枢神经系统 (CNS) 转移的患者;
队列 2:患有难治性疾病和HER2外显子 20 插入或点突变且没有活动性、可测量的 CNS 转移的患者;
队列 3:患有难治性疾病和EGFR或HER2外显子 20 插入或点突变以及可测量的活动性 CNS 转移的患者;
队列 4:初治患者或患有其他EGFR突变(有或没有T790突变、罕见EGFR突变)的难治性疾病患者;
队列 5:先前对 EGFR TKI 有反应的难治性疾病和EGFR外显子 20 插入患者;
队列 6:EGFR外显子 20 插入的初治患者;
队列 7:具有EGFR / HER2突变的难治性疾病和其他肿瘤类型(非 NSCLC)患者;
该试验的第 3 部分包括一个 EXCLAIM 扩展队列,该队列包括 96名先前接受过铂类治疗的EGFR外显子 20 插入阳性患者(n = 86)。
在 2021 年 ASCO 年会上公布的最新数据,患者的客观缓解率(ORR)为28%,疾病控制率(DCR)为78% ,中位缓解持续时间(DoR)为 17.5 个月,中位无进展生存期(PFS)为 7.3 个月,中位总生存期(OS)为 24 个月。
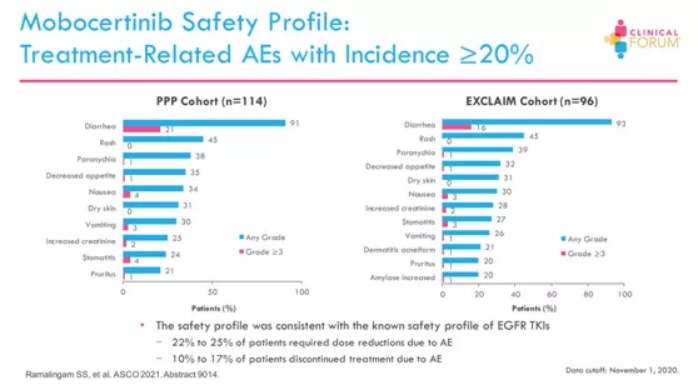
在安全性方面,安全性与EGFR TKI的已知安全性一致,有22%-25%的患者发生了AE,需要调整减少剂量,10%-17%的患者因发生AE停止治疗。
除了两款获批上市的药物,还有一些在研药物展现很好的疗效。
- 上一篇
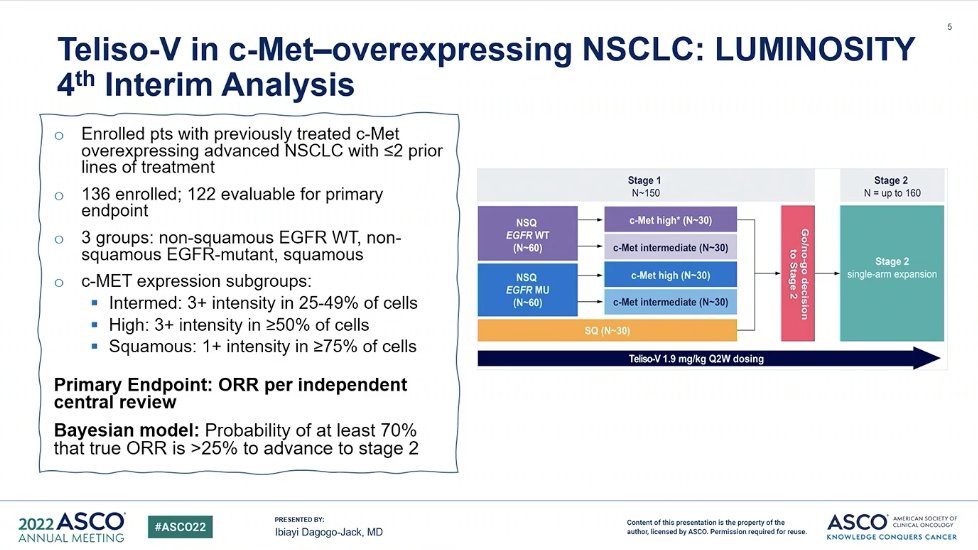
Telistuzumab Vedotin在c-Met过表达的NSCLC中展示出一定的前景
尽管在治疗方面有所进步,但肺癌仍是全球男性和女性癌症相关死亡的主要原因。大约85%的肺癌都归类为非小细胞肺癌(NSCLC)。经过标准护理治疗(包括既往的铂基化疗)后病情进展的患者,治疗选择有限,预后较差。 2022年1月4日,艾伯维公司宣布,美国食品和药物管理局(FDA)授予telisotuzumab vedotin (Teliso-V)突破性治疗资格(BT
- 下一篇

【惜春长恨花开早,玉环飞燕皆尘土】KRAS不佳,SHP2遇挫
1. KRAS G12C联合PD-1治疗1L NSCLC数据不及预期 12月5日,Mirati在ESMO IO会议上发布了KRAS G12C药物Adagrasib联合K药治疗1L NSCLC的数据。在单药2L NSCLC基本失去me-better可能性的情况下,这个联用方案已经成为具有价值的最重要支柱。 https://s27.q4cdn.com/14041

