Dato-DXd横空出世,为NSCLC带来惊艳结果!
第一三共与阿斯利康联手在ADC药物开发方面,取得突破性进展,刚刚在HER2阳性和弱阳性的乳腺癌的治疗方面,Enhertu(DS-8201)惊艳全球!见:NEJM:新型HER2-ADC Enhertu打破HER2低表达的乳腺癌治疗困境(DESTINY-Breast04)。FDA也提前加速批准,见:FDA提前4个月加速批准DS-8201治疗HER2低表达乳腺癌,超6成乳腺癌患者均能受益。DS-8201的成功主要可能源自于单抗与deruxtecan的组合,第一三共在这一ADC平台方面具有领先优势。同时,Enhertu (trastuzumab deruxtecan) 在HER2阳性的NSCLC中也取得漂亮的结果。
最近,第一三共与阿斯利康合作的另一款Datopotamab deruxtecan,专门设计的 TROP2导向 DXd 抗体药物偶联物(ADC)。在2021年欧洲医学肿瘤学会(ESMO)乳腺癌在线会议(ESMOBreast21)上公布了TROP2靶向抗体偶联药物(ADC)datopotamab deruxtecan(Dato-DXd;DS-1062)TROPION-PanTumor01 I期试验三阴性乳腺癌(TNBC)队列的首批数据:在接受标准疗法后出现疾病进展的转移性TNBC患者中,datopotamab deruxtecan显示出非常有前景的初步治疗反应(总缓解率ORR=43%)和疾病控制(DCR=95%)。
最新又公布在NSCLC上的研究结果,同样惊艳!
TROPION-Lung02 Ib 期试验的初步结果表明,datopotamab deruxtecan (Dato-DXd) 与 pembrolizumab 联合或不联合铂类化疗在先前未治疗或预治疗、晚期或转移性没有可治疗的基因组改变的小细胞肺癌(NSCLC)。今天在国际肺癌研究协会 2022 年世界肺癌大会 (WCLC) 上的最新报告 (#MA13.07) 上公布了结果。
对正在进行的 TROPION-Lung02 试验进行的一项期中分析表明,在接受 datopotamab deruxtecan 和 pembrolizumab(双联疗法)治疗的患者中,患者总体缓解率 (ORR) 为 37%(中位随访时间为 6.5 个月);在接受 datopotamab deruxtecan、pembrolizumab 和铂类化疗(三联疗法)的患者中,ORR 为 41%(中位随访 4.4 个月)。在总体人群中,双联和三联联合治疗的疾病控制率 (DCR) 均为 84%。
进一步分析显示,在先前未治疗的患者中,接受双联治疗人群中ORR达到 62%(13 名患者中有 8 名),接受三联治疗组的ORR为 50%(20 名患者中的 10 名)。在接受双联治疗的患者中观察到 8 个部分缓解 (PR),在接受三联治疗的患者中观察到 10 个 PR(三个待确认)。双联治疗的 DCR 为 100%,三联治疗的 DCR 为 90%。
同时,datopotamab deruxtecan 的组合显示出可耐受的安全性,这支持正在进行的研究中的进一步评估。在双联组和三联组中,分别有 40% 和 60% 的患者发生 3 级或更高级别的治疗中出现的不良事件 (TEAE)。在双联组和三联组中最常见的任何级别的 TEAE 分别是口腔炎(56% 和 29%)、恶心(41% 和 48%)、食欲下降(28% 和 38%)、疲劳(25% 和 36%) ) 和贫血 (16% 和 36%)。在两个队列中,有四个间质性肺病(ILD)事件被独立裁决委员会确定为与药物相关;两个被裁定为 1/2 级事件,两个被裁定为 3 级事件。没有 4 级或 5 级 ILD 事件被判定为与药物相关。在数据截止时,有三个潜在的 ILD 事件等待裁决。发生了 3 例死亡(2 例在双联组中,1 例在三联组中),均未确定为与药物相关。不到 22% 的患者因不良事件而中断治疗,13% 的患者发生 datopotamab deruxtecan 剂量中断。
在双联队列中,患者之前接受过一种中线治疗,包括铂化疗(60%)和免疫治疗(30%)。在三联治疗组中,患者之前接受过铂类化疗(35%)和免疫治疗(38%)。以 Datopotamab deruxtecan 为基础的组合作为第一线治疗分别占双联组和三联组患者的 33% 和 63%。截至 2022 年 5 月 2 日数据截止,分别有 53% 和 77% 的患者继续接受双联治疗和三联治疗。
TROPION-Lung02试验结果小结
|
总人群 |
||
|
|
Doublet (n=40) |
Triplet (n=48) |
|---|---|---|
|
Median Follow-Up |
6.5 months |
4.4 months |
|
Efficacy Measure |
Doublet (n=38) |
Triplet (n=37) |
|
ORR, % (confirmed and pending)1 |
37% |
41% |
|
DCR, %2 |
84% |
84% |
|
As 1st-Line Therapy |
||
|
Efficacy Measure |
Doublet (n=13) |
Triplet (n=20) |
|
ORR, %1 |
62% |
50% |
|
PR, % (confirmed) |
62% |
35% |
|
PR, % (pending confirmation) |
0% |
15% |
|
DCR, %2 |
100% |
90% |
|
As 2nd- or Later-Line Therapy |
||
|
Efficacy Measure |
Doublet (n=25) |
Triplet (n=17) |
|
ORR, % (confirmed and pending)1 |
24% |
29% |
DCR, disease control rate; ORR, overall response rate; PR, partial response; CR, complete response; SD, stable disease
1ORR is CR + PR
2DCR is CR + PR + SD
约翰霍普金斯大学西布利纪念医院 Sidney Kimmel 癌症中心医学肿瘤学临床主任、约翰霍普金斯大学医学院肿瘤学副教授Benjamin Philip Levy 医学博士,也是TROPION-Lung02 试验的研究员说:“许多晚期患者非小细胞肺癌在初始治疗后仍会出现疾病进展,这凸显了对新治疗方法的需求。 TROPION-Lung02 试验的初步结果显示,当 datopotamab deruxtecan 和 pembrolizumab 联合或不联合铂类化疗时,疗效和安全性令人鼓舞,值得在一线转移环境中进一步研究。”
阿斯利康首席医疗官兼肿瘤学首席开发官 Cristian Massacesi 表示:“基于今年早些时候分享的 datopotamab deruxtecan 联合治疗三阴性乳腺癌的初步结果,这些来自 TROPION-Lung02 的初步结果反映了联合治疗的更广泛前景。现有的抗体药物偶联物治疗方法。我们期待继续这项重要的研究,旨在为晚期非小细胞肺癌患者提供一种新的、有效的治疗选择。”
Daiichi Sankyo 肿瘤学研发全球负责人 Gilles Gallant 表示:“这些来自 TROPION-Lung02 的早期发现很有希望,代表了第一个报告将 TROP2 导向的 ADC 与免疫结合的结果的肺癌试验。检查点抑制剂联合或不联合铂类化疗用于晚期或转移性非小细胞肺癌患者。这些数据支持 TROPION-Lung08 III 期试验的启动,以进一步评估 datopotamab deruxtecan 联合 pembrolizumab 作为晚期非小细胞肺癌患者的一线联合治疗,而没有可操作的基因组改变。”
1. Siegel R, et al. Cancer Statistics 2021. CA Cancer J Clin. 2021;71:7-33.
2. Centers for Disease Control and Prevention and National Cancer Institute. U.S. Cancer Statistics Working Group. U.S. Cancer Statistics Data Visualizations Tool, based on 2021 submission data (1999-2019); www.cdc.gov/cancer/dataviz, released in June 2022.
3. Hardstock F, et al. Real-world treatment and survival of patients with advanced non-small cell lung Cancer: a German retrospective data analysis. BMC Cancer. 2020;20(1):260.
4. Shields MD, et al. Immunotherapy for Advanced Non–Small Cell Lung Cancer: A Decade of Progress. Am Soc Clin Oncol Educ Book. 2021;41:1-23.
5. Walsh RJ, et al. Resistance to immune checkpoint inhibitors in non-small cell lung cancer: biomarkers and therapeutic strategies. Ther Adv Med Oncol. 2020;12:1758835920937902.
6. World Health Organization. International Agency for Research on Cancer. Lung Fact Sheet. Accessed August 2022.
7. Chen R, et al. Emerging Therapeutic Agents for Advanced Non-Small Cell Lung Cancer. J Hematol Oncol. 2020;13(1):58.
8. Majeed U, et al. Targeted therapy in advanced non-small cell lung cancer: current advances and future trends. J Hematol Oncol. 2021; 14(1): 108.
9. Adib E, et al. Variation in Targetable Genomic Alterations in Non-Small Cell Lung Cancer by Genetic Ancestry, Sex, Smoking History, And Histology. Genome Med. 2022; 14(1): 39.
10. Bubendorf L, et al. Nonsmall cell lung carcinoma: diagnostic difficulties in small biopsies and cytological specimens: Number 2 in the Series “Pathology for the clinician” Edited by Peter Dorfmüller and Alberto Cavazza. Eur Respir Rev. 2017; 26(144): 170007.
11. Paz-Ares L, et al. A Randomized, Placebo-Controlled Trial of Pembrolizumab Plus Chemotherapy in Patients With Metastatic Squamous NSCLC: Protocol-Specified Final Analysis of KEYNOTE-407J. Thorac Oncol. 2020 Oct;15(10):1657-1669.
12. Mok TSK, et al. Pembrolizumab versus chemotherapy for previously untreated, PD-L1-expressing, locally advanced or metastatic non-small-cell lung cancer (KEYNOTE-042): a randomised, open-label, controlled, phase 3 trial. Lancet. 2019 May 4;393(10183):1819-1830.
13. Brahmer J.R. et al. KEYNOTE-024 5-year OS update. ESMO 2021 Virtual Congress. 2021 Sept 16 – 20; Abstract LBA51.
14. Rodríguez-Abreu D et al. Pemetrexed plus platinum with or without pembrolizumab in patients with previously untreated metastatic nonsquamous NSCLC: protocol-specified final analysis from KEYNOTE-189. Ann Onc. 2021 Jul;32(7):881-895.
15. McDougall ARA, et al. Trop2: From Development to Disease. Devel Dynamics. 2015; 244: 99-109.
16. Shvartsur A, et al. Trop2 and its overexpression in cancers: regulation and clinical/therapeutic implications. Genes Cancer. 2015; 6 (3-4): 84-105.
17. Inamura K, et al. Oncotarget. 2017; 8(17):28725-28735. Inamura K, et al. Association of tumor TROP2 expression with prognosis varies among lung cancer subtypes. Oncotarget. 2017; 8(17): 28725-28735.
18. Goldenberg DM, et al. The emergence of trophoblast cell-surface antigen 2 (TROP-2) as a novel cancer target. Oncotarget. 2018; 9(48): 28989-29006.
19. Mito R, et al. Clinical impact of TROP2 in non-small lung cancers and its correlation with abnormal p53 nuclear accumulation. Pathol Int. 2020; 70(5): 287-294.
20. Zaman S, et al. Targeting Trop-2 in solid tumours: future prospects. Onco Targets Ther. 2019; 12: 1781-1790.
21. American Cancer Society. Targeted Drug Therapy for Non-Small Cell Lung Cancer. Available at: https://www.cancer.org/cancer/lung-cancer/treating-non-small-cell/targeted-therapies.html. Accessed July 2022.
22. https://www.businesswire.com/news/home/20220808005728/en/Datopotamab-Deruxtecan-Based-Combinations-Show-Promising-Clinical-Activity-in-Patients-with-Advanced-Non-Small-Cell-Lung-Cancer
23. https://www.astrazeneca.com/media-centre/press-releases/2022/datopotamab-deruxtecan-based-combinations-show-promising-clinical-activity-in-patients.html
- 上一篇
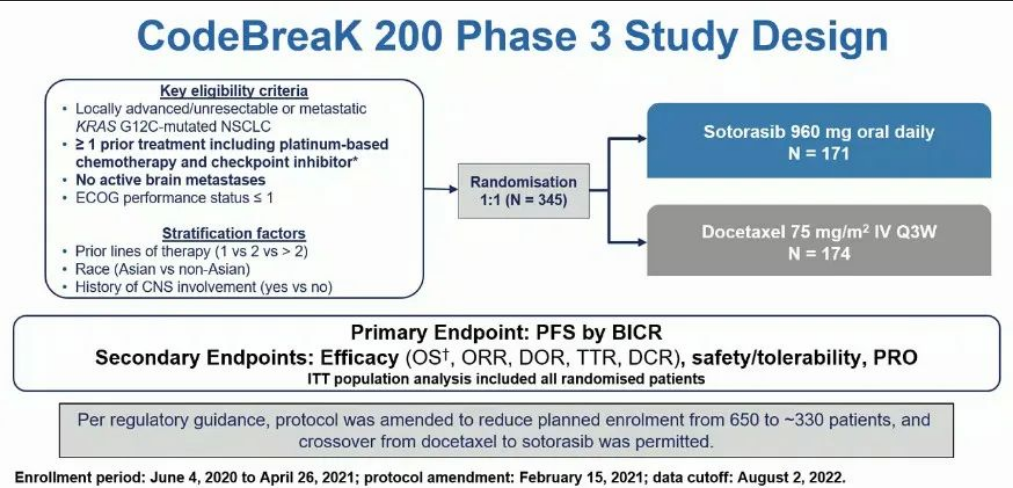
ESC 2022:靶向KRAS G12C Sotorasib治疗NSCLC首个III期结果公布,ORR为28.1%
KRAS是最常见的致癌基因,在多种癌症中均有突变(常见有结肠癌和肺癌、胆管癌、小肠癌、皮肤癌、膀胱癌和乳腺癌等癌症,其中胰腺癌突变率高达90%)。而刚刚召开的2022年欧洲肿瘤内科学会年会(ESMO)上发布了三项有关KRAS靶点相关的临床试验结果,由此可见,KRAS仍是肿瘤领域的研究热点。 索托雷塞治疗NSCLC首个III期结果公布 2022年8月31号,安
- 下一篇
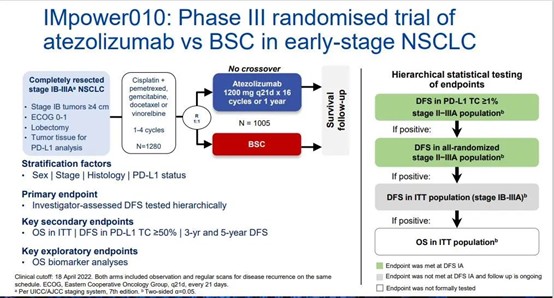
IMpower010研究生存数据首次公布,夯实阿替利珠单抗为标准辅助治疗方案!| WCLC 2022速递
IMpower010 (NCT02486718)的既往数据表明,在铂类化疗后切除的NSCLC患者中,阿替利珠单抗与最佳支持治疗(BSC)相比,无病生存(DFS)有统计学显著获益:PD-L1肿瘤细胞(TC)≥1% II-IIIA患者(DFS HR=0.66),II-IIIA患者(DFS HR=0.79)。基于这些发现,在美国、中国和其他国家,阿替利珠单抗

