Advanced Science | 天津医科大学郝继辉等团队合作发现CD73通过非核苷酸酶依赖性机制促进胰腺癌的转移
2022-12-27肝胆胰肿瘤
CD73是一种细胞表面结合的核苷酸酶,通过将5′-AMP水解为腺苷来促进细胞外腺苷的形成。研究表明,CD73在免疫逃逸、细胞增殖和肿瘤血管生成中起着重要作用,成为癌症治疗的潜在靶标。然而,CD73酶抑制剂的临床应用效果不佳,表明其在肿瘤进展中的作用机制比预期更复杂,需进一步研究。
2022年12月23日,天津医科大学郝继辉、Chang Antao及Tang Bo共同通讯在Advanced Science 在线发表题为“CD73, a Promising Therapeutic Target of Diclofenac, Promotes Metastasis of Pancreatic Cancer through a Nucleotidase Independent Mechanism”的研究论文,该研究发现CD73在胰腺导管腺癌(PDAC)细胞的细胞质中过表达,并以核苷酸酶非依赖性方式促进转移,且不能被CD73单克隆抗体或小分子酶抑制剂抑制。此外,CD73通过与E3连接酶TRIM21结合,与转录抑制因子Snail竞争其结合位点,从而促进PDAC的转移。
CD73转录抑制剂双氯芬酸是一种非甾体抗炎药,在治疗PDAC转移方面比CD73阻断抗体更有效。双氯芬酸还增强了吉西他滨在自发性KPC (LSL-KrasG12D/+,LSL-Trp53R172H/+,Pdx-1-Cre)胰腺癌模型中的治疗效果。因此,对于转移性PDAC,双氯芬酸单独或与以吉西他滨为基础的化疗方案联合使用时,可能是一种有效的抗CD73疗法。

胰腺导管腺癌(PDAC)是最致命的恶性肿瘤之一,主要由快速复发或转移引起,预后效果不佳。由于PDAC缺乏早期症状,约80-85%的患者在疾病局部晚期或转移后才被诊断出来。即使在那些接受根治性手术切除且肿瘤边缘清晰(R0)的患者中,也有75%的患者在术后5年内因复发和转移而死亡。尽管肿瘤转移机制方面已经取得了重大研究进展,但PDAC侵袭和转移扩散的确切分子机制仍不清楚。因此,该研究尝试确定驱动转移性PDAC的关键因素,并制定有效的治疗策略。
CD73(也称NT5E,胞外-5核苷酸酶)催化细胞外腺苷单磷酸 (AMP) 转化为膜透性腺苷,是缺氧或炎症的关键反应。研究表明CD73在多种人类癌症中高度表达,且促进肿瘤免疫逃避,因此被认为是免疫检查点介质。此外,由于CD73参与肿瘤发生、转移、增殖、凋亡逃逸、血管生成和化疗耐药性,已被证明是癌症治疗的关键靶点。
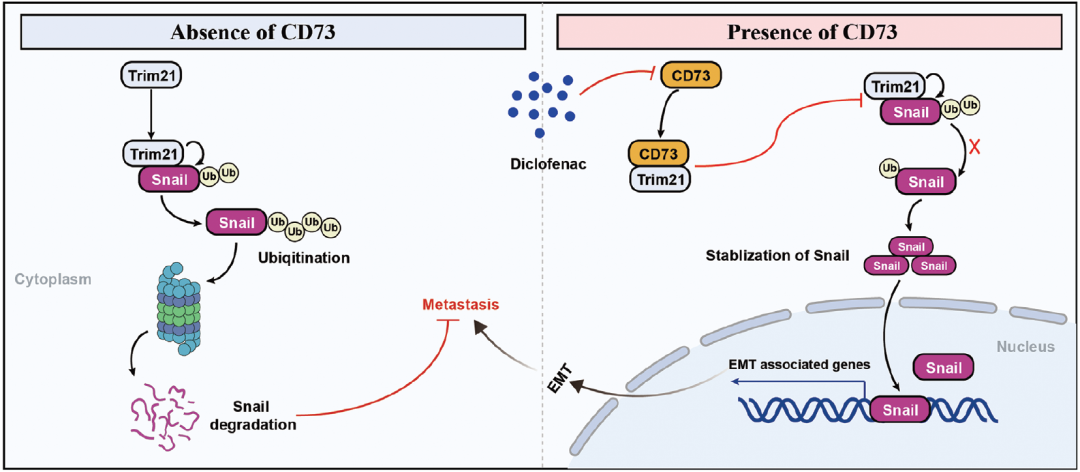
文章模式图(摘自Advanced Science )
近年来,CD73的高效抑制剂数量有所增加,包括单克隆抗体(mAb)和直接抑制其核苷酸酶活性的小分子。临床前研究表明,CD73阻断与基于免疫检查点抑制剂(ICB)的免疫疗法联合,具有用于多种类型癌症的治疗潜力。几种CD73抑制剂目前正在进行针对PDAC(NCT04148937,NCT04572152,NCT03454451,NCT04672434,NCT03616886,NCT03875573等)在内的各种恶性肿瘤的临床试验评估,然而其中一些试验的临床效果有限且受到争议,这表明CD73在肿瘤进展中的作用机制比预期的要复杂。
最近的几项研究表明,CD73作为PDAC的预后生物标志物发挥作用,并通过增强免疫逃避和治疗耐药性来促进肿瘤进展。然而,CD73在PDAC的生物学作用和潜在机制仍不清楚。该研究表明CD73主要位于PDAC细胞的细胞质中,与E3泛素连接酶TRIM21结合,与转录抑制因子Snail防止其被蛋白酶体降解,从而促进上皮-间质转化(EMT)和PDAC的转移扩散。
值得注意的是,CD73对于PDAC的促癌作用与其核苷酸酶活性无关。因此,无论是抗体还是抑制CD73酶活性的小分子都不能有效阻止该过程。此外,研究表明双氯芬酸(一种常用于缓解疼痛、肌肉骨骼疾病、偏头痛、发烧和急性痛风的非甾体抗炎药)显著抑制CD73转录。双氯芬酸单独使用或与一线化疗药物吉西他滨联合使用,均可显著抑制PDAC转移。因此,该研究确定了CD73介导PDAC转移的新型非常规机制,并开发了一种新的靶向策略来提高抗CD73治疗的疗效。
参考消息:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202206335
很赞哦! ()


