前[研]速递,作者解读 | 李贵森教授携中国血磷管理现状登顶Sci Rep,开启CKD患者血磷管理新时代
我国是全球慢性肾脏病(CKD)患者最多的国家1,据统计,我国CKD患病率为10.8%,约有1.2亿CKD患者,已成为重大公共卫生问题2。CKD患者常合并多种并发症,其中高磷血症是最常见的并发症之一,发病率随CKD病情进展不断升高,在CKD 5期非透析患者中高达27.1%3。多项研究证实,高磷血症与CKD进展、心血管(CV)事件发生及全因死亡相关,极大增加患者疾病负担4-6。
在此背景下,我国于2019年发布首部《中国慢性肾脏病矿物质和骨异常诊治指南》,以指导我国CKD患者血磷水平的规范化管理7。时隔3年,如今我国CKD患者的血磷管理现状如何?未来如何进一步改进管理流程并提高管理水平?为此,我们特邀四川省人民医院肾内科主任李贵森教授就以上问题进行深入探讨和分析,以飨读者。
1.基于循证证据,明确中国CKD-MBD管理现状
目前我国慢性肾脏病矿物质与骨异常(CKD-MBD)的管理现状尚不明确,基于2017年KDIGO国际指南8与2019年中国CKD-MBD管理指南更新指导,现将一项全国性调查与一项来自中国四川地区的真实世界研究相结合,对比中国东部发达地区与西部地区研究数据,同时对比四川地区真实世界研究与DOPPS5研究结果,以明确中国CKD-MBD的管理现状9。
1.1 研究设计
一项全国性调查在全国21个省市272家透析中心进行问卷调查,了解各中心接受血液透析(HD)≥3个月的CKD患者,收集各透析中心的患者人数、平均透析龄、血清Ca、P和全段甲状旁腺激素(iPTH)的估计达标率,以及为管理血清iPTH和血清P水平服用药物的估计患者比例。同时对比中国西部四川地区和东部发达地区的血清Ca、P、iPTH估计达标率。
此外,在四川地区进行的一项真实世界研究纳入2020年7月1日至2021年6月30日在四川省肾脏疾病医疗质量信息管理系统登记、至少接受一次血清Ca、P、iPTH检测、年龄>18岁的维持性血液透析(MHD)患者。收集患者ID、性别、年龄、血钙、血磷、iPTH、血红蛋白、白蛋白水平。评估每例患者在研究期间收集的最后一次透析前数据。校正Ca计算为血清Ca(mmol/L)+0.02×(40-血清白蛋白)。采用分光光度法测定血清P、Ca含量。采用免疫化学发光法测定iPTH含量。
以上研究均采用2017年KDIGO更新指南和2019年中国CKD-MBD指南中的推荐指标为治疗目标(表1)。P<0.87 mmol/L和P>1.45 mmol/L分别定义为低磷血症和高磷血症。
表1 2017年KDIGO指南和2019年中国CKD-MBD指南中的推荐指标
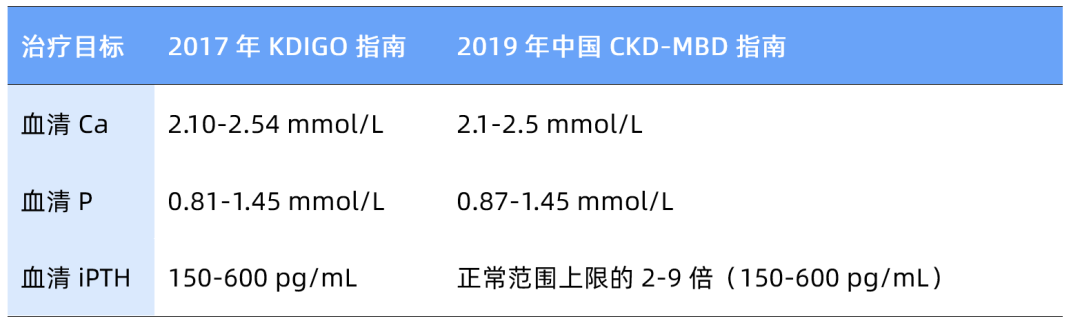
1.2 研究结果
全国性调查共纳入来自全国21个省份,272个透析中心的51,039例MHD患者。血清Ca (2.1-2.5 mmol/L)、P(1.13-1.78 mmol/L)、iPTH(150-600 pg/mL)的估计达标率分别为57.1%、41.1%和52.0%。相比中国东部发达地区,四川地区的血清iPTH估计达标率显著更低,血清Ca估计达标率也较低,血清P差异无统计学意义(表2)。
表2 全国性调查中国西部四川地区与中国东部发达地区各指标达标率对比
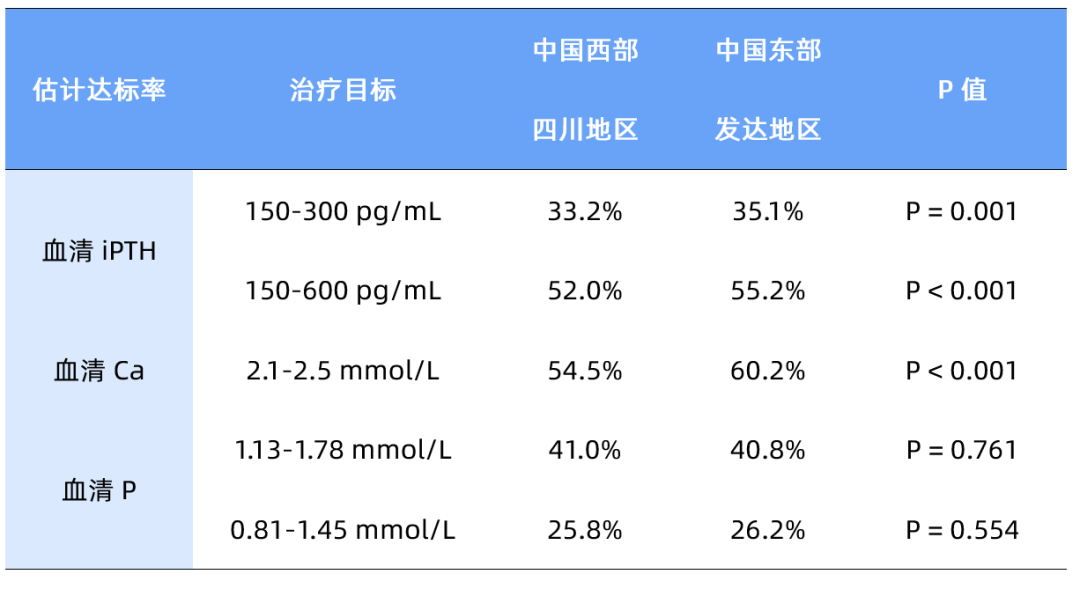
在CKD-MBD管理的药物服用方面,中国30.5%(83/272)的中心口服骨化三醇使用率>60%,40.8%(111/272)的中心口服阿法骨化醇使用率<10%,82.7%(225/272)、88.6%(241/272)和55.9%(152/272)的中心报告静脉注射骨化三醇、帕立骨化醇或拟钙剂使用率低于10%。61.4%(167/272)的中心含钙磷结合剂使用率低于50%,150个(55.1%)中心非含钙磷结合剂使用率<30%。尽管含铝磷结合剂使用率<10%,但仍有90.4%(246/272)的中心使用。
来自四川地区的真实世界研究共纳入7053名HD患者,4,195名(59.5%)患者为男性,5,099名(72.3%)患者在三级医院接受治疗。所有患者的中位年龄为55(47,67)岁。校正后血清Ca、P、iPTH中位水平分别为2.21(2.05,2.37)mmol/L、1.78(1.40,2.18)mmol/L和314.3(164.0,560.0)pg/mL。根据2019年中国CKD-MBD指南,校正后血清Ca、P、iPTH达标率分别为57.6%、24.3%和55.0%。相比欧洲与北美地区DOPPS5结果,四川地区校正后血清Ca和血清P达标率较低,血清iPTH达标率相比欧洲地区无显著差异,但低于北美地区(表3)。相比中国DOPPS5结果,四川地区校正后血清Ca达标率较低,血清P与血清iPTH达标率无组间差异(表4)。
表3 四川地区真实世界研究与欧洲和北美地区DOPPS5研究结果对比
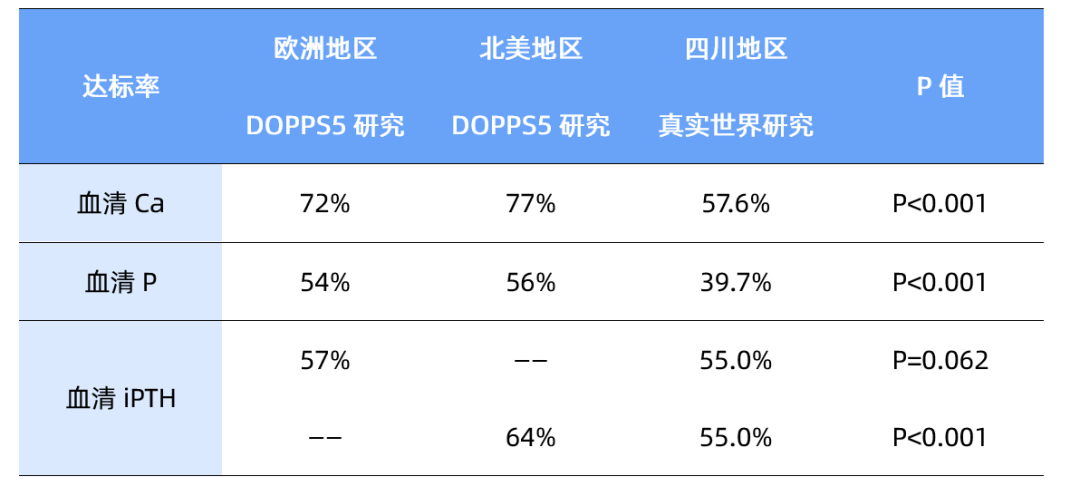
表4 四川地区真实世界研究与中国DOPPS5研究结果对比
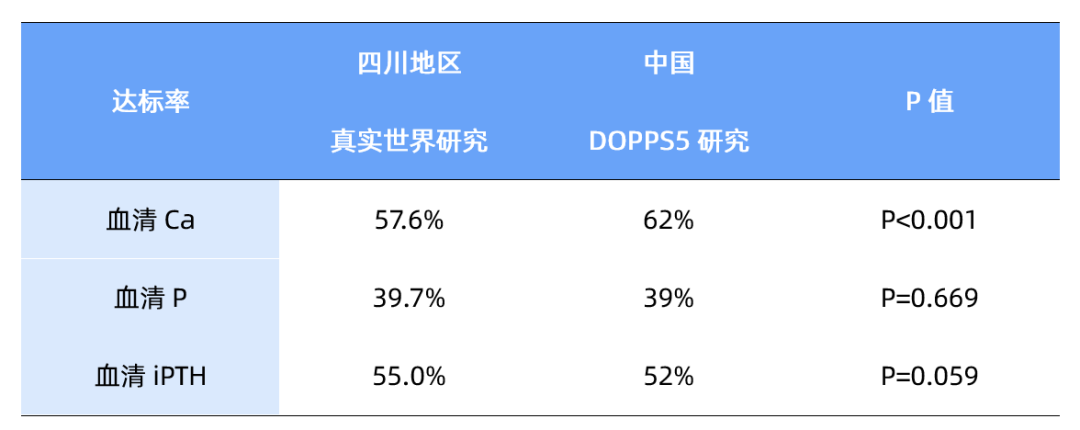
此外,相比三级医院,二级和其他医院校正后血清P与血清Ca达标率较低,高磷血症发生率较高(表5)。男性和女性患者校正后血清Ca、P达标率(P>0.05)差异无统计学意义,男性血清iPTH达标率高于女性患者。年龄>60岁患者校正后血清P(29.0% vs. 22.4% vs. 19.9%,P<0.001)和血清iPTH(57.6% vs. 53.5% vs. 53.3%,P<0.001)高于其他组患者,血清Ca水平组间差异无统计学意义(P>0.05)。
表5 三级医院与二级和其他医院的各指标达标率及高磷血症发生率对比
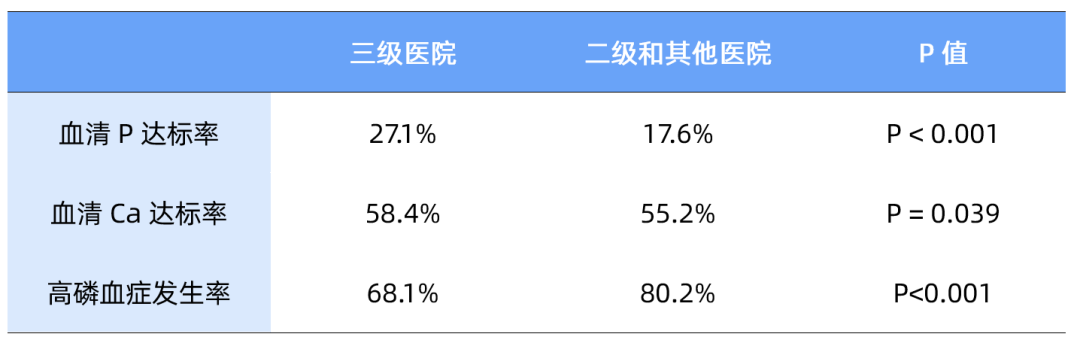
该研究表明,中国MBD各参数指标的达标率,尤其是血清P达标率较低。未来需加强二级和其他医院及年轻透析患者的血磷水平管理。
2.中国血磷管理水平落后,与美国及日本等发达国家相比差距巨大
基于上述研究,我国对于CKD患者血磷水平的管理情况不容乐观,那么,美国与日本等发达国家的血磷管理现状如何?中国相比这些发达国家是否存在差距呢?
2.1血磷管理具有地区差异,美国CKD患者血清P水平明显高于日本
最新研究表明,美国CKD患者的心血管疾病(CVD)发生率高于日本,考虑到高磷血症可能增加CVD的患病风险,或可解释这种差异。为了阐述美国与日本CKD患者中血清P水平的差异10,最新发表在美国肾脏病学杂志(AM J NEPHROL)的一项对比研究比较了美国与日本CKD患者的血清P及相关指标。研究通过使用来自美国和日本全国性、多中心、CKD队列研究的基线数据,在慢性肾功能不全-美国队列研究(CRIC,N=3,870)和慢性肾脏病-日本队列研究(CKD-JAC,N=2,632)中,统一测量方法,对比横断面模型中磷酸盐代谢或血清P、成纤维细胞生长因子-23(FGF23)、以及甲状旁腺素(PTH)等临床指标。为促进估计肾小球滤过率(eGFR)与关注参数间的非线性关系,研究使用限制性立方样条(RCS)建模分析eGFR,其中包含5个内部节点(在CRIC和CKD-JAC合并人群的5、25、50、75和95个百分位),并进行多变量线性回归分析。结果显示,在所有eGFR水平上,CRIC的血清P水平均明显高于CKD-JAC,并且随着eGFR的下降,队列间的差异明显增加。该研究表明,在CKD的所有阶段,CRIC的血清P水平均明显高于CKD-JAC,这可能证实了CKD患者的血清P水平与CVD发病风险存在国际差异,即美国CKD患者血清P水平明显高于日本。
2.2 中国血清P水平居首位,或主要与磷结合剂使用不足相关
此外,一项对于欧洲、亚洲、中东和北美国家继发性甲状旁腺功能亢进(SHPT)的实验室参数和管理模式进行的分析显示,血清P水平>7.0 mg/dL的发生率在法国、英国、和西班牙最低,在中国最高(图1),这可能反映了中国有效磷酸盐结合剂的使用率较低。该分析结果与一项针对中国透析患者的横断面研究结果一致,中国人群中未受控制的高磷血症十分常见,这有可能与高磷饮食、大多数透析中心缺乏营养学家支持,以及磷酸盐结合剂使用不足相关11。
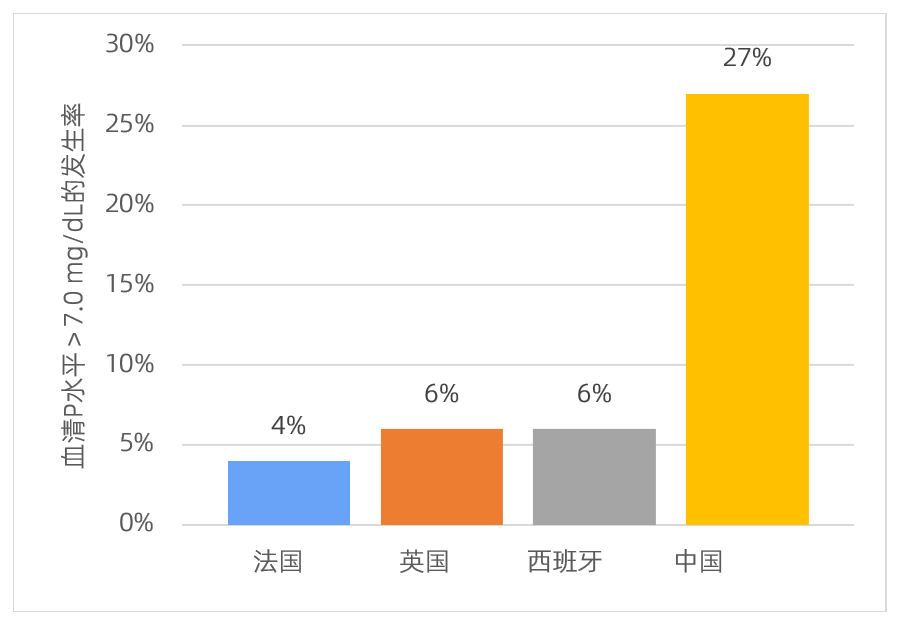
图1 血清P水平>7.0 mg/dL的发生率对比
以上研究表明,美国CKD患者的血清P水平明显高于日本,而中国CKD患者的血清P水平又远高于欧美、日本等发达国家,证实中国血磷管理水平与美国及日本等发达国家存在一定差距,未来还需不断提高。
3.中国血磷管理现状与指南推荐指标相距甚远,亟需规范化诊疗以改善患者预后
3.1中国CKD-MBD指南就血磷管理指标做出推荐
2019年中国CKD-MBD指南特别指出规范化诊断和管理血磷的重要性,考虑到大量证据提示高磷血症的危害较大,指南基于循证证据,结合国际指南更新情况,并充分考虑我国的现状及可行性后,将血磷的控制目标值定为“接近正常”(0.87-1.45mmol/L)7。
3.2 中国血磷管理现状相比指南推荐指标不容乐观
然而目前我国CKD患者血磷管理现状并不乐观,与指南推荐的血磷管理指标存在巨大差距。研究显示,我国血液透析/腹膜透析患者的血磷检测率分别为48.67%和65.19%12,透析患者的血磷达标率为41.5%(目标范围:3.5-5.5mg/dl),远低于发达国家达标水平(54.2%)13。此外,在用药方面,我国CKD患者磷结合剂的使用现状也不乐观,研究显示14,血磷水平为0.96-1.62mmol/L的患者,未使用磷结合剂的患者比例达79.7%,在诊断为高磷血症的CKD患者中,高达71.6%的患者未使用磷结合剂治疗。
3.3 严格遵循指南,规范血磷诊疗
鉴于血磷在CKD进展中的重要作用以及我国CKD患者血磷管理的严峻形势,亟需严格遵循指南,早期加强CKD患者的血磷管理,并进行规范化诊疗,以改善患者生存预后及生活质量。
2019年中国CKD-MBD指南强调,对于血磷管理应重点关注综合管理,即需要综合运用饮食、透析、药物和SHPT管理手段,使患者获得更好的疗效及预后。此外,在降磷药物选择方面,不同于2013年的诊治指导,中国指南不再将含钙磷结合剂作为优先选择,考虑到血管及软组织钙化的预防,特别提出要限制含钙磷结合剂的使用,但在具体的药物选择上,考虑到患者的具体情况和预期寿命,又特别提出了个体化方案的建议7。
目前临床常用降磷药物为磷结合剂,主要包括3种类型:含铝磷结合剂、含钙磷结合剂、不含钙的磷结合剂(如碳酸司维拉姆等)。其中,含钙磷结合剂较为常用,但可导致高钙血症和血管钙化,2019年中国CKD-MBD指南特别提出对其进行限制;含铝磷结合剂长期使用存在铝中毒(如骨软化、脑病等)风险;非钙磷结合剂如碳酸司维拉姆的降磷疗效显著,还可通过延缓钙化等方式间接降低CV风险。
一项多中心、开放标签、单臂、剂量滴定研究15,纳入46例确诊高磷血症的非透析CKD患者,使用碳酸司维拉姆治疗8周。结果显示,相比基线,患者平均血磷水平从2.0 mmol/L降至1.55 mmol/L(P<0.001),降幅达0.45mmol/L,证实碳酸司维拉姆在CKD患者中降磷效果显著。此外,有研究显示16,碳酸司维拉姆治疗52周,不会引起冠状动脉和主动脉钙化的进展,而含钙磷结合剂则显著增加患者冠状动脉钙化(P=0.002)和主动脉钙化(P<0.0001)风险,证实碳酸司维拉姆可明显降低患者血管钙化风险。整体而言,碳酸司维拉姆的临床疗效显著且安全性良好,是CKD患者血磷管理的优选治疗方案。
总结
CKD患者常合并高磷血症,而高磷血症与CKD进展、CV事件发生及全因死亡相关,其危害不容忽视。我国血磷管理现状不容乐观,与美国及日本等发达国家产生巨大差距,2019年中国CKD-MBD指南应运而生,指导规范化诊断和管理CKD患者血磷水平,改善患者生存预后。指南特别提出要限制含钙磷结合剂的使用,而新型非含钙磷结合剂(如碳酸司维拉姆)能够有效控制血磷水平,且不升高血钙,安全性良好,是CKD患者血磷管理的优选治疗方案。

李贵森
· 主任医师,教授,博士生导师
· 电子科技大学附属四川省人民医院肾脏内科主任
· 中华肾脏病学会常委
· 四川省肾脏病专业委员会主任委员
· 中国肾脏康复专业委员会副主任委员
· 四川肾脏康复专业委员会主任委员
· 中国研究型医院学会血液净化专业委员会常委
· 全国卫生计生系统先进工作者,天府名医,省学术技术带头人
· 主持主研各级基金30余项,其中四川省青年创新团队1项,国家级基金7项;近年来在国内外核心期刊上发表论文200余篇,其中SCI收录60余篇。获得多项奖励。
参考文献:
1.中华医学会结核病学分会. 慢性肾脏病合并结核病的治疗专家共识(2022版) [J] . 中华结核和呼吸杂志, 2022, 45(10) : 996-1008. DOI: 10.3760/cma.j.cn112147-20220327-00241.
2.Zhang L, Wang F, Wang L, el at. Prevalence of chronic kidney disease in China: a cross-sectional survey[J]. Lancet. 2012 Mar 3;379(9818):815-22.
3.Zhou C, Wang F, Wang JW, el at. Mineral and Bone Disorder and Its Association with Cardiovascular Parameters in Chinese Patients with Chronic Kidney Disease[J]. Chin Med J (Engl). 2016 Oct 5;129(19):2275-80.
4.Bozic M, Diaz-Tocados JM, Bermudez-Lopez M, el at. Independent effects of secondary hyperparathyroidism and hyperphosphataemia on chronic kidney disease progression and cardiovascular events: an analysis from the NEFRONA cohort[J]. Nephrol Dial Transplant. 2022 Mar 25;37(4):663-672.
5.Torres PU, Troya MI, Dauverge M, el at. Independent effects of parathyroid hormone and phosphate levels on hard outcomes in non-dialysis patients: food for thought[J]. Nephrol Dial Transplant. 2022 Mar 25;37(4):613-616.
6.Merhi B, Shireman T, Carpenter MA, el at. Serum Phosphorus and Risk of Cardiovascular Disease, All-Cause Mortality, or Graft Failure in Kidney Transplant Recipients: An Ancillary Study of the FAVORIT Trial Cohort[J]. Am J Kidney Dis. 2017 Sep;70(3):377-385.
7.国家肾脏疾病临床医学研究中心. 中国慢性肾脏病矿物质和骨异常诊治指南.人民卫生出版社 2019:1-198.
8.KDIGO. Clinical practice guideline update for the diagnosis, evaluation, prevention, and treatment of chronic kidney disease mineral and bone disorder (CKD-MBD). Kidney. Int. Suppl. 7, 1–59.
9.Zhan Y, He X, Hong D,et al . The current status of chronic kidney disease-mineral and bone disorder management in China[J]. Sci Rep. 2022 Oct 6;12(1):16694.
10.Fujii N, Hamano T, Hsu JY, et al . A Comparative Study of Serum Phosphate and Related Parameters in Chronic Kidney Disease between the USA and Japan[J].Am J Nephrol. 2022 ; 53(2-3): 226–239
11.Cozzolino M, Shilov E, Li Z, el at. Pattern of Laboratory Parameters and Management of Secondary Hyperparathyroidism in Countries of Europe, Asia, the Middle East, and North America[J]. Adv Ther. 2020 Jun;37(6):2748-2762.
12.Zhang L, et al. Kidney Int Suppl (2011). 2020 Dec;10(2):e97-e185.
13.Zhao X, Niu Q, Gan L, et al. Baseline data reportof the China Dialysis Outcomes and Practice Patterns Study (DOPPS)[J]. Sci Rep.2021;11(1):873.
14.Zhou C, Wang F, Wang JW, et al. Mineral and BoneDisorder and Its Association with Cardiovascular Parameters in Chinese Patientswith Chronic Kidney Disease[J]. Chin Med J (Engl). 2016;129(19):2275-80.
15.Ketteler M, Rix M, Fan S, et al. Efficacy andtolerability of sevelamer carbonate in hyperphosphatemic patients who havechronic kidney disease and are not on dialysis[J]. Clin J Am Soc Nephrol.2008;3(4):1125-30.
16.Chertow GM, Raggi P, McCarthy JT, et al. Theeffects of sevelamer and calcium acetate on proxies of atherosclerotic andarteriosclerotic vascular disease in hemodialysis patients[J]. Am J Nephrol.2003;23(5):307-314.
MAT-CN-2232292
- 上一篇
由眼观肾,眼底成像或可无创预测ESKD的发生风险
既往结果显示,眼底成像检查结果与人体自然衰老密切相关,可以准确预测死亡和神经退行性疾病的发生、发病风险。值得注意的是,终末期肾脏病(ESKD)的发病率也与自然衰老相关。那么,眼底成像能否无创预测患者的ESKD发病风险呢? 2022年12月5日,多国多学科(肾内科、眼科、计算机)研究团队发现,眼底成像检查结果不仅与自然衰老相关,也与ESKD的发病风险相关。与其
- 下一篇

一表总结,CKD患者营养治疗最新进展
既往研究表明,低蛋白饮食(LPD)可以延缓慢性肾脏病(CKD)患者的肾病进展。目前有三种代表性的LPD食谱,它们分别为蛋奶素食、纯素食以及杂食。然而,这三种食谱各有利弊,并且既往研究的结果并不一致。因此,对于CKD患者而言,究竟哪种食谱更加安全,同时,是否需要补充膳食补剂,以避免营养不良呢? 2022年11月29日,美国专家在Journal of Renal

